ÓXIDOS ÁCIDOS O ANHÍDRIDOS
Son compuestos binarios oxigenados que se forman por la combinación de los no metales con el oxigeno.
Estos compuestos son también conocidos como anhídridos.
NOTA:
Primero se escribe el símbolo del no metal y a continuación el oxigeno, se intercambian los estados de oxidación y se simplifica.
Reacción química: No Metal+ + O-2 Oxido Ácido o Anhídrido
NOMENCLATURA
TRADICIONAL: 1) Se escribe el nombre Anhídrido
2)El nombre del no metal con prefijos y subfijos específicos
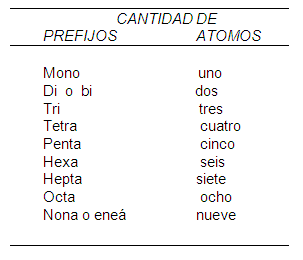
SISTEMÁTICA O IUPAC: Se utilizara los prefijos numéricos (mono,di....) seguido de la palabra oxido y del nombre del no metal.
SISTEMÁTICA O IUPAC: Se utilizara los prefijos numéricos (mono,di....) seguido de la palabra oxido y del nombre del no metal.
STOCK: Se nombrara con la palabra oxido seguido del numero de oxidación del no metal escrito entre paréntesis y en números romanos
EJEMPLOS
TRADICIONAL SISTEMÁTICA STOCK
Cl1 +O-2àCl2O Anhídrido hipoclóroso monoxido de di cloro oxido de cloro (I)
FORMULA DESARROLLADA
Cl---O---Cl
TRADICIONAL SISTEMÁTICA STOCK
Br3+O-2à Br2O3 Anhídrido bromoso Trióxido de di bromo Oxido de bromo (III)
FORMULA DESARROLLADA
Br==O
|
O
|
Br==O

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.